Erhalten Sie vollen Zugriff mit einem kostenfreien Konto
Vorteile von Coloplast® Professional
![]() Erhalten Sie vollen Zugriff auf alle Inhalte, Veranstaltungen und Materialien
Erhalten Sie vollen Zugriff auf alle Inhalte, Veranstaltungen und Materialien
![]() Verfolgen Sie Ihren Fortschritt
Verfolgen Sie Ihren Fortschritt
![]() Teilen Sie unterstützendes Material mit Ihrem Patienten
Teilen Sie unterstützendes Material mit Ihrem Patienten
![]() Teilen Sie Inhalte mit Ihren Kollegen
Teilen Sie Inhalte mit Ihren Kollegen

Tiefes vorderes Resektionssyndrom (engl. Low Anterior Resection Syndrome - LARS)
Gestörte Darmfunktion (Stuhinkontinenz und/oder Verstopfung) kann nach chirurgischer Resektion des Rektums auftreten und die Lebensqualität beeinträchtigen.
Im Jahr 2018 gab es weltweit 1,8 Millionen Fälle von Dickdarmkrebs.1 Fortschritte in der Chirurgie und Strahlentherapie für Patienten mit Dickdarmkrebs haben zu einem besseren Überleben und Bewusstsein für postoperative Ergebnisse geführt.2 Das tiefe vordere Resektionssyndrom (engl. Low Anterior Resection Syndrome - LARS) wird als gestörte Darmfunktion nach chirurgischer Resektion des Rektums definiert, was oft zu einem Nachteil in der Lebensqualität führt.3 Die Symptome reichen von der Stuhlinkontinenz und Drang, zu Verstopfungs- und Entleerungsschwierigkeiten.2,3
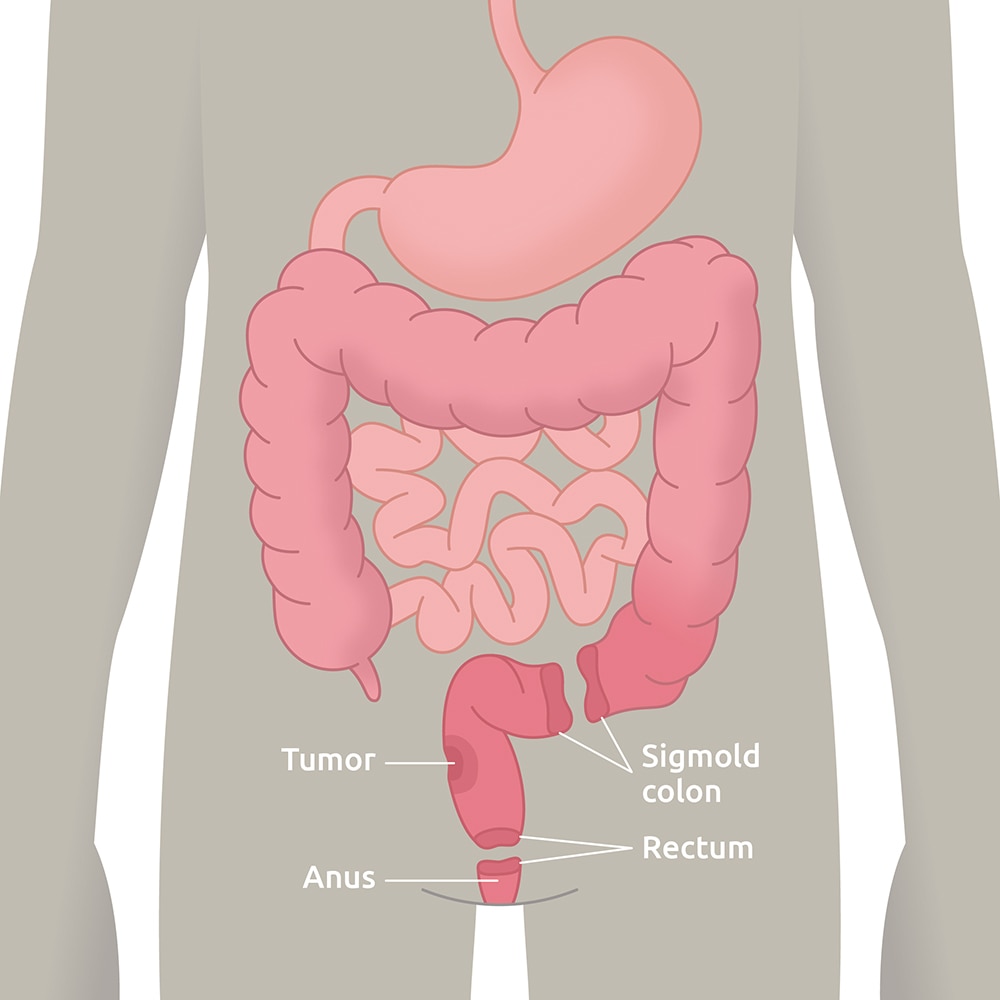
Ätiologie
Wenn ein kranker oder betroffener Teil des Darms entfernt wird, werden die restlichen Abschnitte des Darms operativ wieder miteinander verbunden.
Diese chirurgische Verbindung wird als Anastomose bezeichnet, und es gibt mehrere Arten:
- Colon-rectal
- Colon-anus
- J-pouch
Infolgedessen nimmt das rektale Reservoir an Größe ab und erhöht die Wahrscheinlichkeit einer Stuhlinkontinenz.4
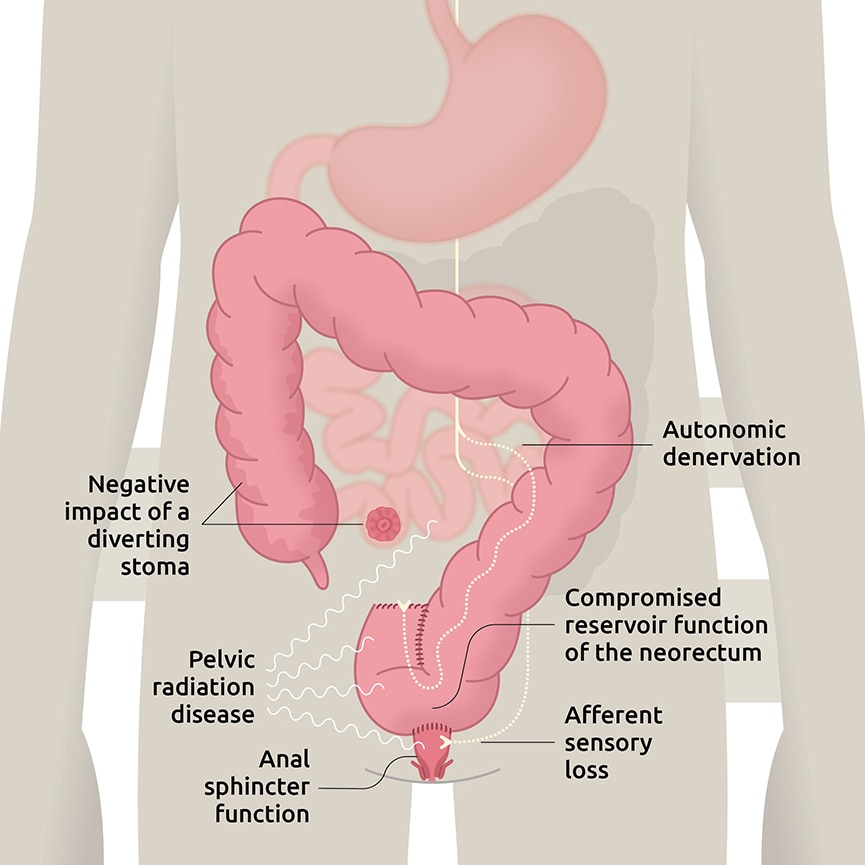
Pathophysiologie
Die chirurgische Resektion des Rektums und die kompromittierten physiologischen Eigenschaften des Neorectums gelten als Hauptursache für LARS. Gründe sind die Änderung der Reservoirfunktion und der beeinträchtigten Evakuierung.5,6 Die Länge des rektalen Überbleibsels korreliert mit besseren funktionellen Ergebnissen, aber diese positive Wirkung geht bei Patienten verloren, die eine vorherige neoadjuvante Therapie erhalten haben.7 Der sensorische Verlust führt zu einer verminderten Diskriminierung von Gas und Stuhl und kann häufige Toilettenbesuche verursachen.8 Ein temporäres Stoma, das zur Vermeidung eines anastomotischen Lecks nach der Operation angelegt wird, kann auch das Risiko von LARS erhöhen, obwohl die Daten widersprüchlich sind.9-11 Denervation von parasympathischen und sympathischen Input erhöht die Beweglichkeit im proximalen Dickdarm und unterbricht Rückkopplungssignale im distalen Dickdarm, die den Transit regulieren.12
Im Jahr 2021 veröffentlichte das LARS Expert Advisory Panel MANagement gUidelinEs für Low Anterior Resection Syndrome MANUEL). Lesen Sie die Publikation hier
LARS Score
Der LARS-Score ist ein validiertes Instrument, um Leistungserbringer im Gesundheitswesen bei der Bestimmung des Schweregrades von LARS in Bezug auf Darmstörungen zu unterstützen.
Transanale Irrigation (TAI) und LARS
Laden Sie sich unten eine kurze Zusammenfassung der klinischen Evidenz von Peristeen bei LARS herunter.;
Referenzen
- World Health Organization, 2019. Cancer: Key Facts, 2019. https://www.who.int/en/news-room/fact-sheets/detail/cancer (accessed March 2020).
- Keane C., et al. 2020. International Consensus Definition of Low Anterior Resection Syndrome. Colorectal Dis. 2020 Mar;22(3):331-341.
- Bryant, et al. 2012. Anterior resection syndrome. Lancet Oncol. 2012;13:e403-408.
- Buzatti KCLR & Petroianu A. Pathophysiological aspects of the low anterior resection syndrome for treatment of rectal cancer. Rev Col Bras Cir. 2017;44(4):397-402.
- Machado M, et al. Functional and physiologic assessment of the colonic reservoir or side-to-end anastomosis after low anterior resection for rectal cancer: a two-year follow-up. Dis Colon Rectum. 2005;48(1):29-36.
- Parc Y, et al. Better Function With a Colonic J-Pouch or a Side-to-end Anastomosis?: A Randomized Controlled Trial to Compare the Complications, Functional Outcome, and Quality of Life in Patients With Low Rectal Cancer After a J-Pouch or a Side-to-end Anastomosis. Ann Surg. 2019 May;269(5):815-826.
- Bondeven P, et al. Neoadjuvant therapy abolishes the functional benefits of a larger rectal remnant, as measured by magnetic resonance imaging after restorative rectal cancer surgery. Eur J Surg Oncol. 2015;41(11):1493-9.
- Haas S, et al. Cortical processing to anorectal stimuli after rectal resection with and without radiotherapy. Tech Coloproctol. 2020;24(7):721-730.
- Floodeen H, et al. Evaluation of long-term anorectal function after low anterior resection: a 5-year follow-up of a randomized multicenter trial. Dis Colon Rectum. 2014;57(10):1162-8.
- Gadan S, et al. Does a Defunctioning Stoma Impair Anorectal Function After Low Anterior Resection of the Rectum for Cancer? A 12-Year Follow-up of a Randomized Multicenter Trial. Dis Colon Rectum. 2017;60(8):800-806.
- Keane C, et al. Functional outcomes from a randomized trial of early closure of temporary ileostomy after rectal excision for cancer. Br J Surg. 2019;106(5):645-652.
- Sakr A, et al. Assessment and management of low anterior resection syndrome after sphincter preserving surgery for rectal cancer. Chin Med J. 2020;133(15):1824-1833.
